Литиевые батарейки - Оптовая продажа
Литиевые батарейки оптом
Если вы оптовый покупатель и представляете магазин или торговую точку (в Москве), то наша компания предлагает Вам батарейки оптом по низким ценам. Ассортимент батареек (элементов питания), фонарей, аккумуляторов и зарядных устройств, предлагаемый нашей компанией "Альфа+Беттерис", достаточно обширен. В продаже имеются батарейки, аккумуляторы, зарядные устройства, адаптеры, фонари, лампы для фонарей, электротовары.
Наша компания предлагает Вам купить батарейки оптом или мелким оптом. Наши цены конкурентоспособны. Среди наших товаров продукция известных брендов. У нас вы найдете Литиевые батарейки различных ценовых категорий.
Классификация элементов питания
Две группы элементов питания - первичные и вторичные
Сейчас все элементы питания делятся на две группы: первичные и вторичные. Суть заключается в том, что первичные элементы работают один раз до полной разрядки, а вторичные (аккумуляторы), можно многократно перезаряжать. Давайте постараемся перечислить элементы каждой группы.
Первичные элементы питания
В первичные входят солевые и щелочные элементы на основе (цинк/диоксид марганца), миниатюрные на основе цинк/диоксид марганца, цинк/оксид серебра, цинк/оксид ртути, воздушно-цинковые, литиевые.
Вторичные - это никель-кадмиевые, никель-металлгидридные и литий-ионные аккумуляторы. Каждая группа имеет определенные параметры.
Солевые батарейки имеют напряжение 1,6 В, щелочные - 1,5 В, аккумуляторы - 1,2 В (здесь и далее под термином "напряжение", если не указано особо, имеется в виду ЭДС - электродвижущая сила). Самым важным параметром элементов питания является ёмкость. От ее величины напрямую зависит продолжительность работы элемента в устройстве. Солевые батарейки имеют наименьшую емкость среди элементов питания, она составляет 400-800 мАч, для щелочных эта величина составляет 1500-3000 мАч, а для аккумуляторов - 750-1500 мАч.
Возникает вопрос - неужели все элементы имеют такую ёмкость? Нет, цифры, приведенные выше, соответствуют так называемому "пальчиковому" типу АА или R6. В связи с этим попробуем теперь разобраться в батареечной номенклатуре.
Чем можно заменить литиевый электрод?
05 марта 2010
Совершенствование литий-ионных батарей не теряет своей актуальности. Причиной тому является, прежде всего, ограниченная удельная емкость материала электрода. Кроме того, сообщалось о недостаточной безопасности литиевого электрода из-за образования литиевых дендритов, которые могут привести к пробою сепаратора. Оба этих фактора побуждают исследователей продолжать поиски альтернативных материалов электрода.
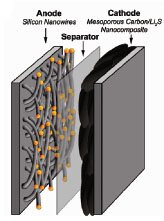
Коллективом исследователей из Стэнфордского университета был предложен выход из сложившейся ситуации. В качестве катода ученые использовали композит, состоящий из сульфида лития и мезапористого углерода, а в качестве электрода кремневые нанонити. Композит Li2S/мезапористый углерод представляет собой гексагонально распределенный массив нанотрубок (толщиной 7-8 нм), разделенные между собой порами (диаметром 3-4 нм), которые заполнены сульфидом лития (рис.1). Этот композиционный материал обладает куда лучшей кинетикой по сравнению с обычным Li2S, что объясняется его строением: сеть углеродных нанотрубок представляет собой проводящую сеть, обеспечивающих доступ к изолятору (Li2S ) в порах, вместе с тем, субмикронный размер частиц углерода уменьшает диффузионный пробег лития. Выбор нанонитей кремния был продиктован долговечностью, а также высокой удельной емкостью.
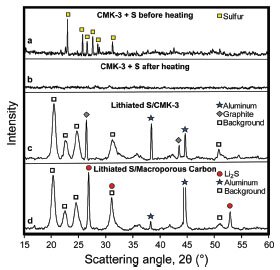
Для получения катода мезопористый углерод (CMK-3) был нагрет с серой до 155 0С, когда вязкость серы минимальна. После того, как под действием капиллярных сил поры в CMK-3 заполнились серой, она была обработана н-бутиллитием для образования сульфида лития. В свою очередь, кремниевые нанонити были получены ПЖК методом, используя силан в качестве прекурсора (рис.2).
Для исследования электрохимических свойств исследователями была собрана полуячейка, в котором в качестве катода использовался Li2S/CMK-3, а электрода – литиевая фольга. Разрядная емкость после первого разряда достигла 573 мАч/г, что составляет 50% от теоретически рассчитанного (в пересчете на полную массу сульфида).
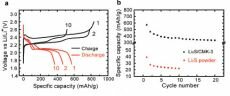
Авторы статьи сравнили электрохимические свойства электрода Li2S/CMK-3 и Li2S с одинаковой массовой долей сульфида лития: ожидаемо обладая одинаковой формой электрохимической кривой, тем не менее, удельная емкость электрода Li2S/CMK-3 на порядок выше, что свидетельствует о существенно лучшей кинетике (рис.3).
Рисунок 1. Схематическое изображение нанокомпозита сульфида лития и мезопористого углерода.
Рисунок 2. РФА анализ нанокомпозита Li2S/CMK-3.
Рисунок 3. а) На графике зависимости напряжения от удельной емкости можно заметить, что напряжение при первой зарядке заметно выше, чем при последующих. Эти кривые обладают нижним плато (соответствующим Li2S2 и Li2S) и нижним плато (соответствующим Li2Sx, 4<x<8). Это свидетельствует о том, что вначале электрохимически активной фазой является смесь Li2S и полисульфидов, улучшающих кинетические показатели катода. Тем не менее, отличие потенциала при первой разрядке лишь в 200 мВ также свидетельствует о том, что нанокомпозит Li2S/CMK-3 обладает хорошими кинетическими свойствами. b) График зависимости удельной емкости от номера цикла.
Источник: Nano Letters
Опубликовал : Шуваев Сергей Викторович
Источник: Нанометр